過去の研究テーマ (クリックすると詳細が表示されます)
1. パラジウム触媒による有機不飽和分子のシアノエステル化反応
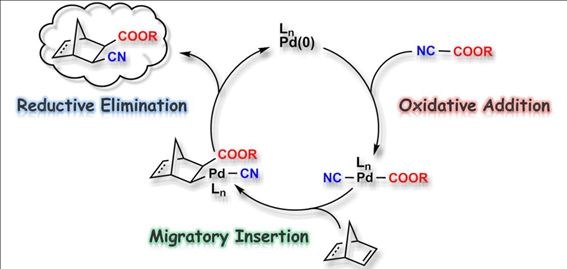
炭素-炭素結合の活性化および続く炭素-炭素多重結合への付加反応は,副生成物を生じることなく原子効率100%で同時に二つの異なる炭素-炭素結合を構築することができるため,有機合成化学において極めて有用な反応です。われわれは,パラジウム触媒を用いることで,ノルボルネン類に極性官能基であるシアノ基とエステル基を同時に導入する反応
(シアノエステル化反応) の開発に成功しました。
この反応は,酸化的付加,移動挿入,還元的脱離を経て進行すると考えています。
-
Y. Nishihara, Y. Inoue, M. Itazaki, and K. Takagi
Palladium-Catalyzed Cyanoesterification of Norbornenes with Cyanoformates via the NC-Pd-COOR (R = Me and Et) Intermediate
Org. Lett. 7, 2639-2641 (2005).
- Y. Nishihara, Y. Inoue, S. Izawa, M. Miyasaka, K. Tanemura, K. Nakajima, and K. Takagi
Cyanoesterification of Norbornenes Catalyzed by Palladium: Facile Synthetic Methodology to Introduce Cyano and Ester Functionalities via Direct Carbon-Carbon Bond Cleavage of Cyanoformates
Tetrahedron 62, 9872-9882 (2006).
- Y. Nishihara, M. Miyasaka, Y. Inoue, T. Yamaguchi, M. Kojima, and K. Takagi
Preparation, Structures, and Thermal Reactivity of Alkoxycarbonyl(cyano)palladium(II) Complexes, trans-Pd(COOR)(CN)(PPh3)2 (R = Me, Et, nPr. iPr, nBu, tBu, and Bn) as Intermediates of the Palladium-Catalyzed Cyanoesterification of Norbornene Derivatives
Organometallics 26, 4054-4060 (2007).
- Jing Li, Shintaro Noyori, Kiyohiko Nakajima, and Yasushi Nishihara
Preparation, Structures, and Thermal Reactivity of Alkoxycarbonyl(cyano)palladium(II) Complexes, trans-Pd(COOR)(CN)(PPh3)2 (R = Me, Et, nPr. iPr, nBu, tBu, and Bn) as Intermediates of the Palladium-Catalyzed Cyanoesterification of Norbornene Derivatives
Organometallics 33, 3500-3507 (2014).
- Jing Li, Yasuhiro Okuda, Jiaji Zhao, Seiji Mori, and Yasushi Nishihara
Skeletal Rearrangement of Cyano-Substituted Iminoisobenzofurans into Alkyl 2-Cyanobenzoates Catalyzed by B(C6F5)3
Org. Lett. 16, 5220-5223 (2014).
2. 直接的炭素―ケイ素結合の活性化による非対称ジアリールエチンの合成
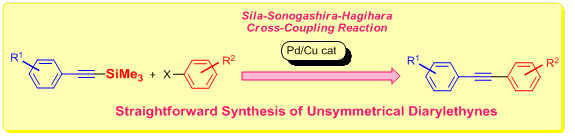
非対称ジアリールエチンは、種々の生理活性物質や有機機能材料などの合成中間体として幅広く用いられている化合物群の一つです。われわれの研究室では、パラジウムや銅などの遷移金属触媒を用いて、アルキニルシランの炭素?ケイ素結合を直接活性化し,有機ハロゲン化物と直接的にカップリング(シラ―薗頭―萩原カップリング反応)させることで、これらの合成中間体の簡便かつ効率的な合成法の開発を達成しています。
-
Y. Nishihara, E. Inoue, Y. Okada, and K. Takagi
Sila-Sonogashira Cross-Coupling Reactions of Activated Aryl Chlorides with Alkynylsilanes
Synlett (19), 3041-3045 (2008).
- Y. Nishihara, E. Inoue, D. Ogawa, Y. Okada, S. Noyori, and K. Takagi
Palladium/Copper-Catalyzed Sila-Sonogashira Reactions of Aryl Iodides with Alkynylsilanes via a Direct C-Si Bond Activation
Tetrahedron Lett. 50(32), 4643-4646 (2009).
- Y. Nishihara, S. Noyori, T. Okamoto, M. Suetsugu, and M. Iwasaki
Copper-Catalyzed Sila-Sonogashira-Hagihara Cross-Coupling Reactions of Alkynylsilanes with Aryl Iodides under Palladium-Free Conditions
Chem. Lett. 40, 972-974 (2011).
- Y. Nishihara, E. Inoue, S. Noyori, D. Ogawa, Y. Okada, and M. Iwasaki
Synthesis of Unsymmetrical Disubstituted Ethynes by the Palladium/Copper(I)-Cocatalyzed Sila-Sonogashira-Hagihara Coupling Reactions of Alkynylsilanes with Aryl Iodides, Bromides, and Chlorides through a Direct Activation of a Carbon-Silicon Bond
Tetrahedron 68, 4869-4881 (2012).
- Y. Nishihara, D. Ogawa, S. Noyori, and M. Iwasaki
Synthesis of Unsymmetrical Diarylethynes by Pd(0)/Cu(I)-cocatalyzed Sila-Sonogashira-Hagihara Coupling Reactions of Alkynylsilanes with Aryl Tosylates or Mesylates
Chem. Lett. 41, 1503-1505 (2012).
- Daisuke Ogawa, Jing Li, Masato Suetsugu, Jiao Jiao, Masayuki Iwasaki, Yasushi Nishihara
Palladium-Free Synthesis of Unsymmetrical Diarylethynes by Cross-Coupling Reaction of Alkynylboronates with Aryl Iodides Catalyzed by CuCl
Tetrahedron Lett. 54, 518-521 (2013).
3. 量子化学計算を用いた反応機構の解明
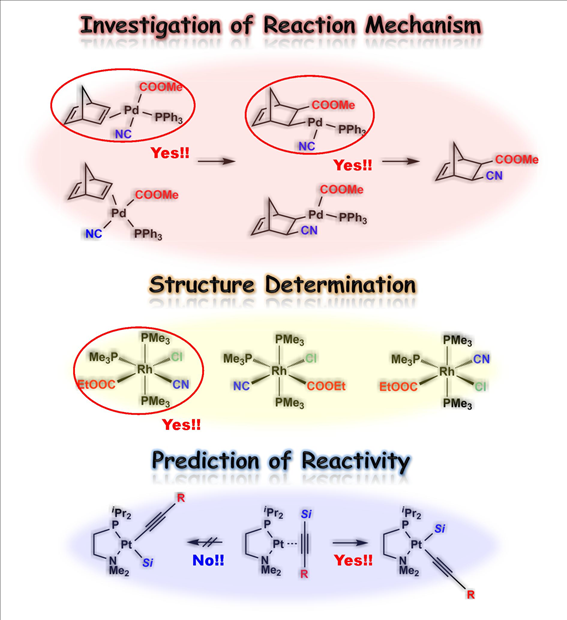
近年の量子化学計算の進歩はめざましく,有機合成系の研究室でも反応機構の解明,生成物の同定などに量子化学計算が活発に用いられています。当研究室でも,Gaussianを用いて,開発したパラジウム触媒によるノルボルナジエンのシアノエステル化の反応機構の解明をはじめとして,様々な有機合成反応について実験だけでなく,理論的にも追及することで,新たな触媒反応を発見するための手掛りとして利用しています。
-
Yasuhiro Okuda, Takeru Okamoto, Arisa Yamamoto, Jing Li, Kiyohiko Nakajima, and Yasushi Nishihara
Synthesis, Structure, and Isomerization of Alkoxycarbonyl(chloro)(cyano)rhodium(III) Complexes, mer-RhCl(CO2R)(CN)(PMe3)3 (R = Me, Et, nPr, iPr, nBu, and Bn) through C-C Bond Cleavage of Cyanoformates
Chem. Lett. 43, 417-419.
-
Yasuhiro Okuda, Yuya Ishiguro, Seiji Mori, Kiyohiko Nakajima, and Yasushi Nishihara
Experimental and Theoretical Studies on the Platinum-Mediated Selective C(sp)-Si Bond Cleavage of Alkynylsilanes
Organometallics 33, 1878-1889 (2014).
4. 触媒的縮環反応を利用した機能性多環芳香族有機分子の合成
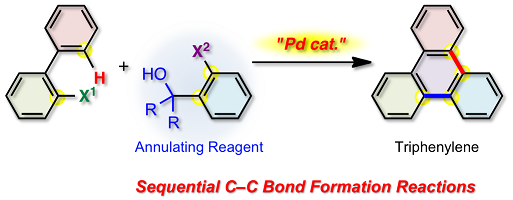
縮環π共役系有機分子は、複数の芳香環が縮合した化合物であり、そのレドックス機能やバンドギャップのため様々な機能の発現が期待される化合物群です。例えば、機能性有機材料として、有機ELディスプレイや有機電界効果トランジスタなどへの応用が望まれています。しかしながら,その合成は容易ではなく,多くの場合には複数の反応工程および過酷な反応条件が必要であるため,低い全収率や官能基許容性が問題となっています。そこで,私たちは,遷移金属触媒触媒を用いて,従来法よりも簡便な操作かつ短工程で目的の縮環パイ共役系有機分子を得ることを目的として研究をおこなっています。現在,パラジウム触媒を用いることで,効率的にトリフェニレンを合成することに成功しています。
-
Masayuki Iwasaki, Shohei Iino, and Yasushi Nishihara
Palladium-Catalyzed Annulation of o-Iodobiphenyls with o-Bromobenzyl Alcohols: Synthesis of Functionalized Triphenylenes via C-C and C-H Bond Cleavages
Org. Lett. 15, 5326-5329 (2013).
5. 遷移金属触媒を用いた炭素-水素結合の直接硫黄化反応の開発
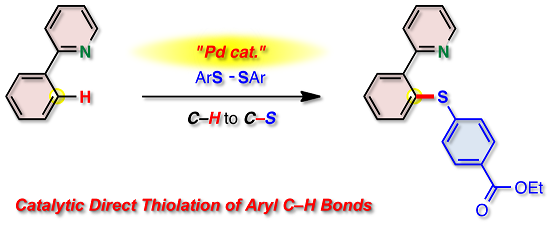
有機硫黄化合物は,薬理活性をもつ化合物や医薬上重要な天然物によく見られ,有機化学において大変重要な化合物群です。高度に官能基化されたアリールスルフィド骨格の代表的な合成法は,ハロゲン化アリールとチオールのクロスカップリング反応です。本反応は,高い官能基許容性を有しているため有用であるものの,ハロゲン化された芳香環を出発物質として用いなければなりません。そのために,多段階の合成過程が必要であり,全収率も低くなります。一方,私たちは,芳香環の炭素-水素結合を直接硫黄化することで,この問題を解決しようとしています。現在,パラジウム触媒がこの炭素-水素結合の直接硫黄化反応に非常に効果的であることを見いだしています。
-
Masayuki Iwasaki, Miki Iyanaga, Yuta Tsuchiya, Yugo Nishimura, Wenjuan Li, Zhiping Li, and Yasushi Nishihara
Palladium-Catalyzed Direct Thiolation of Aryl C-H Bonds with Disulfides
Chem. Eur. J. 20, 2459-2462 (2014).
-
Masayuki Iwasaki, Yuta Tsuchiya, Kiyohiko Nakajima, and Yasushi Nishihara
Chelate-Assisted Direct Selenation of Aryl C-H Bonds with Diselenides Catalyzed by Palladium
Org. Lett. 16, 4920-4923 (2014).
-
Masayuki Iwasaki, Wataru Kaneshika, Yuta Tsuchiya, Kiyohiko Nakajima, and Yasushi Nishihara
Palladium-Catalyzed peri-Selective Chalcogenation of Naphthylamines with Diaryl Disulfides and Diselenides via C-H Bond Cleavage
J. Org. Chem. 79, 11330-11338 (2014).
6. 遷移金属触媒による位置および立体選択的なアルキンのハロチオ化反応
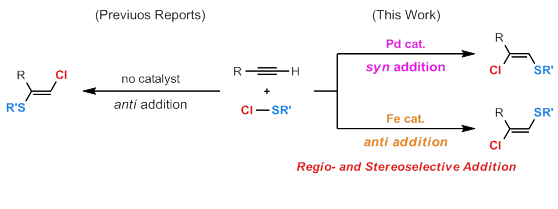
炭素-炭素不飽和結合のビシナル二官能基化反応は,有機不飽和分子に二種類の官能基を一挙に導入することができるため,有機化学において理想的な物質変換法です。とりわけ,ハロゲン-硫黄結合のアルキンへの付加反応は,有用な合成中間体である 2-ハロアルケニルスルフィドを与えるため,これまで盛んに研究がおこなわれてきました。しかしながら,その有用性にも関わらず,これまで反応の位置および立体選択性を制御することはできませんでした。私たちは,パラジウムや鉄のような遷移金属触媒を利用することで,望みの付加体を作り分けることに成功しました。
-
Masayuki Iwasaki, Tomoya Fujii, Arisa Yamamoto, Kiyohiko Nakajima, and Yasushi Nishihara
Palladium-Catalyzed Regio- and Stereoselective Chlorothiolation of Terminal Alkynes with Sulfenyl Chlorides
Chem. Asian J. 9, 58-62 (2014).
-
Masayuki Iwasaki, Tomoya Fujii, Kiyohiko Nakajima, and Yasushi Nishihara
Iron-Induced Regio- and Stereoselective Addition of Sulfenyl Chlorides to Alkynes via a Radical Pathway
Angew. Chem. Int. Ed. 53, 13880-13884 (2014).





